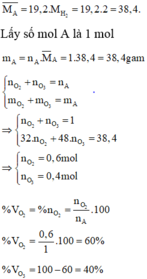Hỗn hợp T gồm O2 và O3 trong đó % khối lượng của O2 trong T bằng 50%. Tỉ khối của T so với He là:

Những câu hỏi liên quan
Một hỗn hợp B (ở đktc) gồm khí O2;N2 và NH3. Biết rằng khối lượng của khí NH3 bằng 7/8 khối lượng khí O2 , khối lượng của khí N2 bằng 1/2 tổng khối lượng của khí O2 và NH3 . Tính thể tích có từng khí trong hỗn hợp B, biết rằng tỉ khối của hỗn hợp B so với khí H2 bằng 13,5
1. Hỗn hợp X gồm H2 , O2 , SOx . Trong hỗn hợp H2 chiếm 50% về thể tích , O2 chiếm 25% còn lại là SOx . Trong hỗn hợp SOx chiếm 64% về khối lượng
a. Xác định công thức hóa học của SOx
b. Tính tỉ khối của X so với O2
chọn số mol hh là 1
=> nH2 = 0.5
nO2 = 0.25
=> n SOx = 0.25
vì thể tích tỉ lệ thuận vs số mol
mặt khác:
m hh = 0.5 * 2 + 0.25 * 32 + 0.25 * (32+16x)
=17+4x
% mSOx= 0.68956
=> [0.25(32+16x)]/(17+4x) = 0.68956
bấm máy giải ra đc x =3
vậy CTHH của SOx là SO3
b/.
với x = 3 khi đó m hh = 17+4*3 = 29
=> dX/O2 = 29/32 =0.90625
Đúng 0
Bình luận (1)
Hỗn hợp X gồm các khí sau :H2,O2 ,SOx .Trong hỗn hợp H2 chiếm 50% về thể tích,O2 chiếm 25% còn lại là SOx.Ttong hỗn hợp SOxchieems 68,956% về khối lượng.
a, Xác định công thức hóa học của SOx
b, Tính tỉ khối của X so với O2
Hỗn hợp X gồm H2 O2 SOx. 6 hỗn hợp H2 chiếm 50% về thể tích O2 chiếm 25% về thể tích còn lại là oxi trong hỗn hợp oxi chiếm 68,956% về khối lượng
a xác định công thức a x
b tính tỉ khối của hỗn hợp so với O2
a) Xét trong 1 (mol) hỗn hợp X
==>\(\left\{{}\begin{matrix}n_{H2}=0,5\left(mol\right)\\n_{O2}=0,25\left(mol\right)\\n_{SOx}=0,25\left(mol\right)\end{matrix}\right.\)
=> mhỗn hợp X = mH2 + mO2 + mSOx = 0,5 x 2 + 0,25 x 32 + 0,25(32+ 16x) = 17 + 4x (gam)
Mặt khác: %mSOx =\(\dfrac{0,25\left(32+16x\right)}{17+4x}=68,956\%\)
=> x = 3
=> CTHH: SO3
b) dSO3/O2 = 8032=2,5
Đúng 0
Bình luận (1)
a, Tính khối lượng mol trung bình của hỗn hợp khí gồm 0,1mol Cl2 và 0,2mol O2
b, Hỗn hợp A có V3,36 (l) gồm Cl2 và O2 với tỉ lệ thể tích là 1:2. Tính khối lượng mol trung bình của hỗn hợp A ( V đktc)
c, Hỗn hợp X gồm Cl2 và O2 có tỉ khối với He là 25,75
+) Tính % về thể tích của mỗi khí trong X
+) Tính % về số mol của mỗi khí trong X
+) Tinh % về khối lượng của mỗi khí trong X
Đọc tiếp
a, Tính khối lượng mol trung bình của hỗn hợp khí gồm 0,1mol Cl2 và 0,2mol O2
b, Hỗn hợp A có V=3,36 (l) gồm Cl2 và O2 với tỉ lệ thể tích là 1:2. Tính khối lượng mol trung bình của hỗn hợp A ( V đktc)
c, Hỗn hợp X gồm Cl2 và O2 có tỉ khối với He là 25,75
+) Tính % về thể tích của mỗi khí trong X
+) Tính % về số mol của mỗi khí trong X
+) Tinh % về khối lượng của mỗi khí trong X
a. Khối lượng mol trung bình của hỗn hợp là:
\(\overline{M}=\dfrac{n_{Cl2}\cdot M_{Cl2}+n_{O2}\cdot M_{O2}}{n_{Cl2}+n_{O2}}=45\)
b. Ta có: nCl2 = 0,05mol và nO2 = 0,1 mol
=> \(\overline{M}=\dfrac{n_{Cl2}\cdot M_{Cl2}+n_{O2}\cdot M_{O2}}{n_{Cl2}+n_{O2}}=45\)
c. Chọn số nCl2 = 1 mol và nO2 = x mol.
Vì tỉ khối của hỗn hợp khí so với He bằng 25,75 suy ra \(\overline{M}=25,75\cdot4=103\)
(Đề câu c sai: Vì MCl2 > \(\overline{M}\) > MO2)
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm có O2 và O3. Tỉ khối của hỗn hợp khí A đối với H2 là 19,2. Phần trăm theo thể tích của O2 và O3 trong hỗn hợp X lần lượt là A. 60% và 40%. B. 40% và 60%. C. 50% và 50%. D. 30% và 70%.
Đọc tiếp
Hỗn hợp khí A gồm có O2 và O3. Tỉ khối của hỗn hợp khí A đối với H2 là 19,2. Phần trăm theo thể tích của O2 và O3 trong hỗn hợp X lần lượt là
A. 60% và 40%.
B. 40% và 60%.
C. 50% và 50%.
D. 30% và 70%.
Hỗn hợp X gồm các khí sau H2 , O2 ,SOn . Trong hỗn hợp H2 chiếm 50% về thể tích, O2 chiếm 25% còn lại là SOx . Trong hỗn hợp SẼ chiếm 64% về khối lượng.
a, xác định công thức hóa học về SOx
b, Tính tỉ khối của X so với O2?
1 mol hỗn hợp X có:
\(\left\{{}\begin{matrix}nH2=0,5\left(mol\right)\\nO2=0,25\left(mol\right)\\nSOx=0,25\left(mol\right)\end{matrix}\right.\)
mhhX=mH2+mO2+mSOx
=0,5.2+0,25.32+0,25(32+16)x
=17+4x
Mặt khác:
%mSOx=\(\dfrac{0,25\left(32+16x\right)}{17+4x}\).100=64
=>x=2
=>CT: SO2
b) dSO2/O2=64/32=2
Đúng 0
Bình luận (2)
hỗn hợp x gồm o2 và o3, 1 thời gian, O3 phân hủy thành O2, thể tích hỗn hợp tăng 4% so với ban đầu. Tính tỉ khối X so với H2
2o3=3o2
Số mol o2 là a
Số mol o3 là b mol nên no2 sinh ra là 1,5b mol
Số mol o2 sau phản ứng là 1,5b+a mol
số mol khí tăng 0,5b mol
0,5b=0,04(a+b)
11,5b=a
Dx/h2=(32a+48b) /(2a+2b) =16,64
Cậu tham khảo đi t không chắc
Đúng 0
Bình luận (0)
Hỗn hợp X gồm (CO2;O2;H2) có % khối lượng của CO2 là 22%, % khối lượng của O2 là 64%, còn lại là H2. Tính % thể tích các khí trong hỗn hợp X và tỉ khối của X so với H2
%H2=100%-22%-64%=14%
- Chọn 1 mol hỗn hợp. Ta có:
\(n_{CO_2}=\dfrac{22.1}{100}=0,22mol\)
\(n_{O_2}=\dfrac{64.1}{100}=0,64\)
\(n_{H_2}=\dfrac{14.1}{100}=0,14mol\)
\(\overline{M}=\dfrac{0,22.44+0,64.32+0,14.2}{1}=30,44\)
\(d_{\dfrac{X}{H_2}}=\dfrac{30,44}{2}=15,22\)
Đúng 0
Bình luận (0)